Luyện tập Liên kết hóa học
16.1.
![]()
A. −3, +3, +5.
B. +3, −3, −5.
C. +3, +5, −3.
D. +4, +6, +3.
16.2.
![]()
A. 0, +4, +3, +8.
B. −2, +4, +6, +8.
C. −2, +4, +4, +6.
D. +2, +4, +8, +10.
16.3.
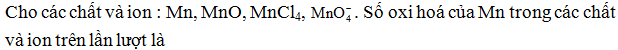
A. +2 , −2, −4, +8.
B. 0, +2, +4, +7.
C. 0, −2, −4, −7.
D. 0, +2, −4, −7.
16.4. Ion nào sau đây có 32 electron ?
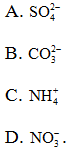
16.5. Ion nào sau đây có tổng số proton bằng 48 ?
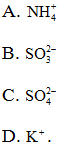
16.6. Cho dãy oxit sau : . Những oxit có liên kết ion là
A. .
B. .
C. .
D. .
16.7. Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là . Trong hợp chất khí của nguyên tố X với hiđro, X chiếm 94,12% khối lượng. Phần trăm khối lượng của X trong oxit cao nhất là
A. 50%.
B. 27%.
C. 60%.
D. 40%.
16.8. Hợp chất khí với hiđro của nguyên tố R có công thức tổng quát là , oxit cao nhất của nguyên tố này chứa 53,3% oxi về khối lượng. Nguyên tố R là
A. cacbon.
B. chì.
C. thiếc.
D. silic.
16.9. Số oxi hoá của clo (Cl) trong hợp chất là
A. +1.
B. −2.
C.+6.
D.+5.
16.10. Hãy tính số oxi hoá của crom (Cr) trong hợp chất .
16.11. Hãy tính số oxi hoá của lưu huỳnh (S) trong hợp chất .
16.12. Hãy cho biết sự khác nhau về liên kết hoá học trong các tinh thể ion, tinh thể nguyên tử và tinh thể phân tử.
16.13. Hãy cho biết sự khác nhau về các cấu tử (các hạt tạo nên tinh thể) trong tinh thể ion, tinh thể nguyên tử, tinh thể phân tử.
16.14. Hãy cho biết sự khác nhau về tính chất giữa tinh thể nguyên tử và tinh thể phân tử.
16.15. Hãy viết công thức cấu tạo của các phân tử: .
Dựa vào quy tắc biến thiên độ âm điện của các nguyên tố trong một chu kì, hãy cho biết trong các phân tử nói trên, phân tử nào có liên kết không phân cực, phân tử nào có liên kết phân cực mạnh nhất.
16.16. Cho dãy oxit sau đây :
.
Biết rằng độ âm điện của các nguyên tố :
Na, Mg, Al, Si, P, S, Cl, O
Lần lượt bằng : 0,93 ; 1,31; 1,61; 1,90; 2,19; 2,58; 3,16; 3,44.
Hãy dự đoán trong các oxit đó thì liên kết trong các oxit nào là liên kết ion, liên kết cộng hoá trị có cực, liên kết cộng hoá trị không cực ?
16.17.
Hãy cho biết số oxi hoá của các kim loại trong các hợp chất sau đây :
.
16.18.
a) Hãy cho biết số oxi hoá của o trong các hợp chất:
.
b) Hãy cho biết trong trường hợp nào thì oxi có số oxi hoá bằng −2, bằng −1, bằng +2.
16.19. Gác cation và anion
đều có cấu hình electron lớp ngoài cùng là
. Xác định vị trí của R, Y, X trong bảng tuần hoàn.
16.20.
Hợp chất MX có tổng số các hạt trong phân tử là 84. Trong nguyên tử M cũng như X, số hạt proton bằng số hạt nơtron. Tổng số electron trong nhiều hơn trong
là 8 hạt. Xác định chất MX.


Comments mới nhất