Bài 40 : ANCOL
40.1. C
40.2.
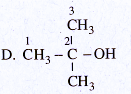
40.3. B
40.4. 1 – D ; 2 – D ; 3 – A
40.5. D 40.6. C 40.7. C
40.8.
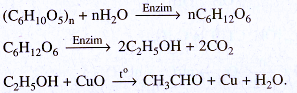
40.9.
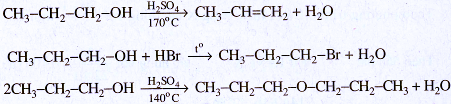
40.10. Ancol no mạch hở là CnH2n+2_x(OH)x ; CTPT là CnH2n+2Ox.
![]()
Theo phương trình : 1,00 mol ancol tác dụng với 3n + 1 – x : 2 mol O2
Theo đầu bài :0,35 mol ancol tác dụng với 31,36 : 22,40 = 1,400 mol O2
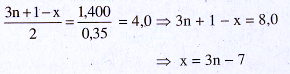
Ở các ancol đa chức, mỗi nguyên tử cacbon không thể kết hợp với quá 1 nhóm OH ; vì vậy 1 ≤ x ≤ n.
1 ≤ 3n – 7 ≤ n
2,67 ≤ n ≤ 3,5 ; n nguyên ⇒ n = 3
⇒ x = 3 x 3 – 7 = 2.
Công thức phân tử : C3H8O2.
Các công thức cấu tạo :
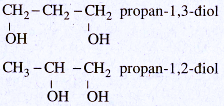
40.11.

40.12. Cách 1 : Giả sử trong 35,60 g hỗn hợp M có x mol CnH2n+1OH và y mol Cn+1H2n+3OH :
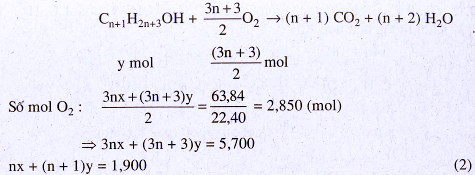
Nhân (2) với 14 : 14nx + (14n + 14)y = 26,60 (2′)
Lấy (1) – (2′) ta được 18x + 18y = 9,00
⇒ x + y = 0,500
Từ (2) : n (x + y) + y = 1,900 ⇒ y = 1,900 – 0,500n
0 < y < 0,500 ⇒ 0 < 1,900 – 0,500n < 0,500 ⇒ 2,80 < n < 3,80
⇒ n = 3 ⇒ y = 1,900 – 1,50 = 0,40 ⇒ x = 0,50 – 0,40 = 0,10.
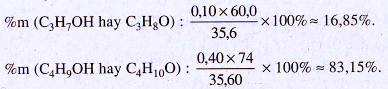
Cách 2 : Đặt công thức của 2 ancol là
![]()
Theo phương trình :(14n + 18)g ancol tác dụng với 3/2 n mol O2
Theo đầu bài : 35,60g ancol tác dụng với 2,850 mol O2
![]()
⇒ Hai ancol là C3H7OH (x mol) và C4H9OH (y mol)
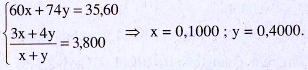
Từ đó tính được phần trăm khối lượng từng chất (như ở trên).
40.13. Cách 1. 1. Hỗn hợp A gồm x mol CnH2n+1OH và y mol CmH2m+1OH. Khối lượng hỗn hợp A là :
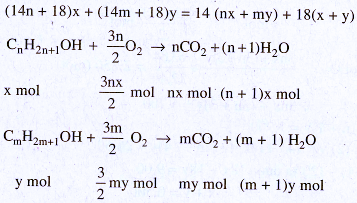
![]()
Hiệu khối lượng của CO2 và của H2O :
44 (nx + my) – 18 [(n + 1)x + (m + 1)y] = 1,88
26 (nx + my) – 18 (x + y) = 1,88 (2)
Từ (1) và (2), tìm được :
x + y = 0,0400.
Khối lượng hỗn hợp A là : 14 x 0,100 + 18 x 0,0400 = 2,12 (g).
2. Vì m = n + 2 ; ta có : nx + (n + 2)y = 0,100
⇒ n(x + y) + 2y = 0,100 → y = 0,0500 – 0,0200n
0 < y < 0,0400 ⇒ 0,500 < n < 2,50
Nếu n = 1, hai ancol là CH3OH và C4H7OH
⇒y = 0,0300 và x = 0,0100
⇒ CH3OH chiếm 15,1% ; C3H7OH chiếm 84,9% khối lượng hỗn hợp A.
Nếu n = 2, hai ancol là C2H5OH và C4H9OH. y = 0,0100 và x = 0,0300.
C2H5OH chiếm 65,1%, C4H9OH chiếm 84,9% khối lượng hỗn hợp A.
Cách 2.1. Công thức chung của hai ancol là CnH2n+1OH và tổng số mol của chúng là a. Khối lượng hỗn hợp : (14 n + 18)a.
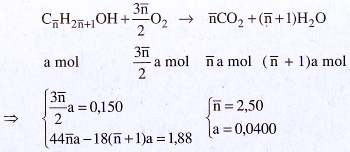
Khối lượng hỗn hợp : (14 x 2,50 + 18) x 0,0400 = 2,12 (g)
2. n < 2,50 < n + 2 ⇒ 0,500 < n < 2,50.
Phần cuối giống như ở cách giải 1.
40.14. Khi 8,12 g A tác dụng với Cu(OH)2 chỉ có 1 phản ứng hoá học :
![]()
Số mol glixerol trong 8,12gA = 2 x số mol Cu(OH)2
= 2 x 1,96 : 98,0 = 0,0400 (mol).
Số mol glixerol trong 20,30 g A là : 0,0400 x 20,30 : 8,12 = 0,100 mol.
Khối lượng glixerol trong 20,30 g A là : 0,100 x 92,0 = 9,20 (g).
Khối lượng R-OH trong 20,30 g A là : 20,30 – 9,20 = 11,10 (g).
Khi 20,30 g A tác dụng với Na có 2 phản ứng hoá học
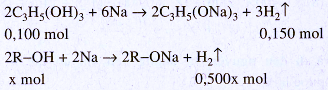
số mol H2 = 0,150 + 0,500x = 5,04 : 22,40 = 0,225 (mol) ⇒ x = 0,150.
Khối lượng 1 mol R-OH : 11,10 : 0,150 = 74,0 (g)
R-OH = 74 ⇒ R = 74 – 17 = 57 ; R là -C4H9
Công thức phân tử : C4H10O
Các CTCT và tên :
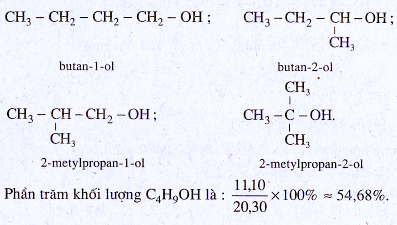
40.15.
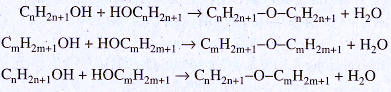
Số mol 3 ete = số mol H2O = 21,6 : 18,0 = 1,20 (mol)
Số mol mỗi ete = 1,20 : 3 = 0,400 (mol).
Khối lượng 3 ete :
(28n + 18) x 0,400 + (28m + 18) x 0,400 + (14n + 14m + 18) x 0,400 = 72,0
⇔ n + m = 3.
Vì n và m đều nguyên và dương nên chỉ có thể n = 1 và m = 2 (hoặc ngược lại).
Hai ancol là CH3-OH và CH3 – CH2 – OH.
Số mol mỗi ancol là 1,2 mol.
Khối lượng CH3OH là : 1,20 x 32 = 38,4 (g).
Khối lượng C2H5OH là : 1,20 x 46 – 55,2 (g).
40.16. 1. Hỗn hợp khí A chứa CnH2n và Cn+1H2n+2 với phân tử khối trung bình là :
1,35 x 28 = 37,8
![]()
⇒ 14n < 37,8 < 14n + 14
1,70 < n < 2,70 ⇒ n = 2.
CTPT của 2 anken là C2H4 và C3H6.
2. Giả sử trong 1 mol hỗn hợp A có x mol C3H6 và (1 – x) mol C2H4 :
42x + 28 (1 – x) = 37,8 ⇒ x = 0,700
Như vậy, trong 1 mol hỗn hợp A có 0,700 mol C3H6 và 0,300 mol C2H4.
Giả sử hiđrat hoá hoàn toàn 1 mol A :
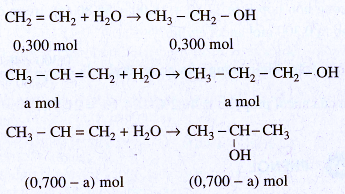
Tỉ lệ khối lượng giữa ancol bậc I so với ancol bậc II:
![]()
Hỗn hợp B gồm 0,300 mol CH3 – CH2 – OH ;
0,200 mol CH3 – CH2 – CH2 – OH và 0,500 mol CH3 – CH-CH3 ;
có khối lượng tổng cộng là 55,80 g.
Phần trăm về khối lượng etanol (ancol etylic) là :
![]()
Phần trăm về khối lượng của propan-l-ol (ancol propylic) là :
![]()
Propan-2-ol (ancol isopropylic) chiếm :
![]()
Riêng câu 2 cũng có thể lập luận như sau :
Phần trăm khối lượng của ancol bậc II (ancol isopropylic) :
![]()
Vậy phần trăm khối lượng của 2 ancol bậc I là 46,2%.
Nếu dùng 1 mol A (37,80 g) thì lượng H20 là 1 mol (18,00 g) và khối lượng hỗn hợp B là 37,80 + 18,00 = 55,80 (g), trong đó 0,300 mol C2H4 tạo ra 0,300 mol ancol etylic.
Phần trăm khối lượng của ancol etylic là
![]()
và của ancol propylic là 46,2% – 24,7% = 21,5%.
Xem thêm Hướng dẫn – Bài Giải – Đáp án – Chương VIII – Bài 41 : PHENOL tại đây

Comments mới nhất