Bài 37 : Nguồn HIĐROCACBON thiên nhiên
37.1. D
37.2. 1 – C ; 2 – D ; 3 – A ; 4 – B.
37.3. 1 – C ; 2 – D ; 3 – B ; 4 – A.
37.4. Khối lượng xăng thu được nhờ chưng cất :
500 x 15 : 100 =75 (tấn).
Khối lượng mazut là : 500 x 60 : 100 = 300 (tấn).
Khối lượng xăng thu được nhờ crăckinh là :
300 x 50 : 100 = 150 (tấn).
Khối lượng xăng thu được tổng cộng là :
150 + 75 = 225 (tấn).
37.5. 1. Trong 1000 m³ khí thiên nhiên có 850 m³ CH4
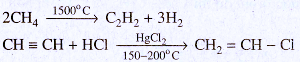
Khối lượng vinyl clorua thu được (nếu hiệu suất các quá trình là 100%) là :
![]()
Với hiệu suất cho ở đầu bài, khối lượng vinyl clorua là
![]()
2. Nhiêt lượng cần dùng để làm nóng 100 lít nước từ 20°C lên 100°C :
100 x 4,18 x (100 – 20) = 33440 (kJ)
Vì 20% nhiệt lượng đã toả ra môi trường nên nhiệt lượng mà khí thiên nhiên cần cung cấp phải là
![]()
Đặt số mol C2H6 là X thì số mol CH4 là 85.10¯¹ x.
Ta có 1560x + 880 x 85.10¯¹x = 41800
x = 462.10‾²
Thể tích khí thiên nhiên cần dùng :
![]()
37.6
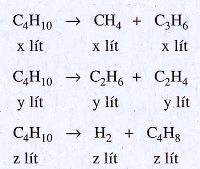
Đặt thể tích C4H10 không tham gia phản ứng là t lít.
2x + 2y + 2z + t = 47,0 (1)
Khi đi qua nước brom dư thì C3H6, C2H4 và C4H8 bị hấp thụ ; thể tích các khí còn lại:
x + y + z + t = 25,0 (2)
Lấy (1) – (2) ta có X + y + z = 22,0 ; đó chính là thể tích C4H10 đã phản ứng, còn x + y + z + t = 25,0 cũng chính là thể tích C4H10 trước phản ứng.
Phần trăm theo thể tích của C4H10 phản ứng : 22,0 : 25,0 x 100% = 88,0%.
2. Giả sử đốt 25,0 lít khí còn lại sau khi qua nước brom :
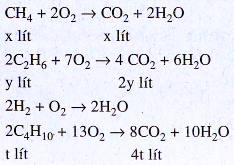
Thể tích CO2 thu được sẽ là :
![]()
Ngoài ra theo đầu bài y = 3x. (4)
Giải hệ (1), (2), (3), (4) ta được x = 5 ; y = 15 ; z = 2 ; t = 3.
Thành phần phần trăm về thể tích của hỗn hợp A :
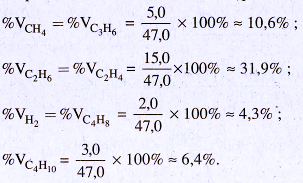

Trackbacks