I.KIẾN THỨC CẦN NHỚ
1Tính chất hóa học của oxit được minh họa bởi những phản ứng hóa học:
CaO (r) + 2HCl (dd) → CaCl2 (dd) + H2O (l)
CO2 (k) + Ca(OH)2 (dd) → CaCO3 (r) + H2O (l)
![]()
CaO (r) + H2O (l) → Ca(OH)2 (dd)
SO2 (k) + H2O (l) → H2SO3 (dd)
2.Tính chất hóa học của axit được minh họa bởi những phản ứng hóa học:
H2SO4 (loãng) + Fe (r) → FeSO4 (dd) + H2 (k)
H2SO4 (dd) + CuO (r) → CuSO4(dd) + H2O (l)
H2SO4 (dd) + 2NaOH (dd) → Na2SO4(dd) + 2H2O (l)
![]()
II.GIẢI BÀI TẬP
Giải Bài 1. Trang 21 sách giáo khoa hóa học 9
a.Tác dụng được với H2O:
CaO + H2O → Ca(OH)2
Na2O+ H2O → 2NaOH
SO2 + H2O →H2SO3
CO2 + H2O -> H2CO3
b.Tác dụng với HCl:
CuO + 2HCl → CuCl2 + H2O
CaO + 2HCl →CaCl2 + H2O
Na2O + 2HCl → 2NaCl + H2O
c.Tác dụng với dung dịch NaOH:
SO2 + 2NaOH → Na2SO3 + H2O
CO2 + 2NaOH → Na2CO3 + H2O
Giải Bài 2. Trang 21 sách giáo khoa hóa học 9
a.Oxit được điều chế bằng phản ứng hóa hợp.
2H2 + O2 → 2H2O
4Na + 5O2 —>2Na2O
4P + 5O2 → 2P2O5
b.Oxit được điều chế bằng phản ứng hóa hợp vá phân huỷ.
2Cu + O2 → 2CuO
![]()
+ O2 → C + O2
![]()
Giải Bài 3. Trang 21 sách giáo khoa hóa học 9
Để loại bỏ được những tạp chất ra khỏi CO, ta cho hỗn hợp trên qua dung dịch Ca(OH)2. Ta có phản ứng:
CO2 + Ca(OH)2 — CaCO3 ↑ + H2O
SO2 + Ga(OH)2 → CaSO3 ↓ + H2O
Vậy CO2 và SO2 được giữ lại. Còn lại CO nguyên chất.
Giải Bài 4. Trang 21 sách giáo khoa hóa học 9
a.Axit suníuric tác dụng với đồng (II) oxit.
CuO + H2SO4 → CuSO4 + H2O (1)
b.Axit sunfuric tác dụng với đồng.
Vì 1 mol CuSO4 sinh ra cần 1 mol H2SO4.
![]()
1 mol CuSO4 sinh ra cần 2 mol H2SO4 nên dùng phản ứng (1) tiết kiệm hơn.
Giải Bài 5. Trang 21 sách giáo khoa hóa học 9
S + O2 → SO2 (1)
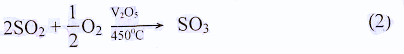
SO2 + 2NaOH → Na2SO3 + H2O (3)
SO3 + H2O → H2SO4 (4)
![]()
SO2 + H2O → H2SO3 (6)
H2SO3 + 2NaOH → Na2SO3 + 2H2O (7)
Na2SO3 + H2SO4→ NaSO4 + SO2 ↑ + H2O (8)
H2SO4 + 2NaOH → Na2SO4 + 2H2O (9)
Na2SO4 + Ba(NO3)2 → BaSO4↓ + 2NaNO3 (10)

Comments mới nhất