Axit sunfuric – Muối sunfat
33.1. Một loại oleum có công thức hoá học là (
).
Số oxi hoá của lưu huỳnh trong hợp chất oleum là
A. +2.
B. +4.
C. +6.
D. +8.
33.2. Chất nào sau đây chỉ có tính oxi hoá ?
A.
B. .
C. .
D. .
33.3. Phân tử hoặc ion có nhiều electron nhất là
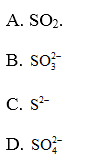
33.4. Hãy ghép từng cặp mỗi chất (ở cột bên trái) với tính chất của chất đó (ở cột bên phải) :

33.5. PTHH của phản ứng lưu huỳnh tác dụng với dung dịch axit sunfuric đặc, nóng :
S + →
+
Trong phản ứng này, tỉ lệ giữa số nguyên tử lưu huỳnh bị khử và số nguyên tử lưu huỳnh bị oxi hoá là
A. 1 : 2.
B. 1 : 3.
C. 3 : 1.
D. 2 : 1.
33.6*. Cho sơ đồ phản ứng :
(đặc, nóng) + Fe →
+
+
Số phân tử bị khử và số phân tử
tạo muối trong PTHH của phản ứng trên là
A. 6 và 3.
B. 3 và 6.
C. 6 và 6.
D. 3 và 3.
33.7. Số mol cần dùng để pha chế 5 lít dung dịch
2M là
A. 2,5 mol.
B. 5,0 mol.
C. 10 mol.
D. 20 mol.
33.8. Nêu phương pháp hoá học để phân biệt các dung dịch sau với điều kiện được dùng quỳ tím và chọn thêm một hoá chất làm thuốc thử :
![]()
Viết PTHH của những phản ứng đã dùng.
33.9. Có những chất khi tham gia phản ứng hoá học này có vai trò là chất khử, nhưng trong phản ứng khác lại có vai trò là chất oxi hoá. Hãy dẫn ra những PTHH để minh hoạ cho những trường hợp sau :
a) Chất đó là oxit.
b) Chất đó là axit.
c) Chất đó là muối.
d) Chất đó là đơn chất.
33.10. Có những chất sau : , dung dịch
đặc, dung dịch
loãng.
Hãy cho biết chất nào tác dụng với dung dịch đặc hay loãng để sinh ra :
a) Chất khí nhẹ hơn không khí và cháy được trong không khí.
b) Chất khí nặng hơn không khí, nó vừa có tính oxi hoá vừa có tính khử.
c) Chất khí nặng hơn không khí và không duy trì sự cháy.
Viết tất cả PTHH cho các phản ứng.
33.11. Trong bài thực hành về tính chất hoá học của axit sunfuric có những hoá chất sau : (đựờng), dung dịch NaOH, giấy quỳ tím, dung dịch
loãng và dung dịch
đặc.
Hãy lập kế hoạch thí nghiệm để chứng minh rằng :
a) Dung dịch loãng có những tính chất hoá học chung của axit
b) Dung dịch đặc có những tính chất hoá học đặc trưng là tính oxi hoá mạnh và tính háo nước.
33.12. Cần điều chế một lượng muối . Phương pháp nào sau đây tiết kiệm được axit sunfuric ?
a) Axit sunfuric tác dụng với đồng(II) oxit.
b) Axit sunfuric tác dụng với kim loại đồng.
33.13. Người ta có thể điều chế một số chất khí bằng những phản ứng hoá học sau :
a) Nhiệt phân .
b) Dung dịch HCl đặc tác dụng với .
c) Dung dịch loãng tác dụng với Zn.
d) Dung dịch đặc tác dụng với Cu.
e) Nhiệt phân .
– Hãy cho biết tên chất khí được sinh ra trong mỗi phản ứng trên và viết PTHH của các phản ứng.
– Bằng thí nghiệm nào có thể khẳng định được chất khí sinh ra trong mỗi thí nghiệm ?
33.14. Thực hiện những biến đổi hoá học sau bằng cách viết những PTHH và ghi điều kiện của phản ứng, nếu có :
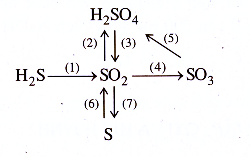 33.15. Dung dịch axit sunfuric đặc (D = 1,83 g/ml) chứa 6,4% nước. Hãy cho biết trong 1 lít dung dịch axit này có bao nhiêu mol
33.15. Dung dịch axit sunfuric đặc (D = 1,83 g/ml) chứa 6,4% nước. Hãy cho biết trong 1 lít dung dịch axit này có bao nhiêu mol ?
33.16. Xử lí 1,143 g hỗn hợp rắn gồm kali clorua và kali sunfat bằng dung dịch axit sunfuric đặc, thu được 1,218 g kali sunfat.
a) Viết PTHH của phản ứng xảy ra.
b) Tính khối lượng eủa mỗi muối trong hỗn hợp rắn ban đầu.
33.17. Cho 7,8 g hỗn hợp hai kim loại là Mg và AI tác dụng với dung dịch loãng, dư. Khi phản ứng kết thúc, người ta thu được 8,96 lít khí (đktc).
a) Viết PTHH của các phản ứng đã xảy ra.
b) Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
c) Tính thể tích dung dịch 2M đã tham gia các phản ứng.
33.18. Cho Fe phản ứng với dung dịch thu được khí A và 11,04 g muối. Tính khối lượng Fe phản ứng biết rằng số mol Fe phản ứng bằng 37,5% số mol
phản ứng.
33.19. Hoà tan hoàn toàn 3,22 g hỗn hợp X gồm Fe, Mg, Zn bằng một lượng vừa đủ dung dịch loãng, thu được 1,344 lít khí
(đktc) và dung dịch chứa m gam muối. Xác định giá trị của m.
33.20. Cho m g hỗn hợp 2 kim loại AI và Cu chia làm 2 phần bằng nhau :
– Phần 1 : Cho tác dụng với dung dịch loãng, dư thu được 1,344 lít khí
(đktc).
– Phần 2 : Cho tác dụng với dung dịeh đặc nóng, dư, thu được 2,24 lít khí
(đktc). Xác định giá trị của m.
33.21. Sau khi hoà tan 8,45 g oleum A vào nước được dung dịch B, để trung hoà dung dịch B cần 200 ml dung dịch NaOH 1M. Xác định công thức của A.




Comments mới nhất