Bài 15 : Định luật bảo toàn khối lượng
15.1.a) Viết công thức về khối lượng cho phản ứng giữa kim loại kẽm và
axit clohiđric HC1 tạo ra chất kẽm clorua Zn và khí hiđro. (Xem lại hình 2.6, trong SGK về phản ứng nàv).
b) Cho biết khối lượng của kẽm và axit clohiđric đã phản ứng là 6,5 g và 7,3 g, khối lượng của chất kẽm clorua là 13,6 g.
Hãy tính khối lượng của khí hiđro bay lên.
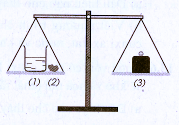
15.2.Biết rằng axit clohiđric có phản ứng với chất canxi cacbonat tạo ra chất canxi clorua, nước và khí cacbon đioxit. Một cốc đựng dung dịch axit clohiđric (1) .và cục đá vôi (2) (thành phần chính là chất canxi cacbonat) được đặt trên một đĩa cân. Trên đĩa cân thứ hai đặt quả cân (3) vừa đủ cho cân ở vị trí thăng bằng ?
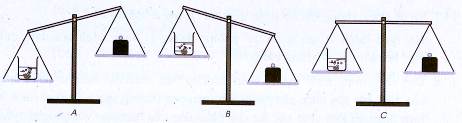
Bỏ cục đá vôi vào dung dịch axit clohiđric. Sau một thời gian phản ứng, cân sẽ ở vị trí nào : A, B hay C ? Giải thích.
15.3. Hãy giải thích vì sao :
a) Khi nung nóng cục đá vôi thì thấy khối lượng giảm đi. (Xem lại bài tập 12.3 về đá vôi trong lò nung vôi).
b) Khi nung nóng miếng đồng trong không khí (có khí oxi) thì thấy khối lượng tăng lên. (Xem bài tập 3, thuộc bài 15, SGK ; khi đun nóng kim loại đọng (Cu) cũng có phản ứng tương tự kim loại magie (Mg)).
15.4.Đun nóng mạnh hỗn hợp gồm 28 g bột sắt và 20 g bột lưu huỳnh thu được 44 g chất sắt(II) sunfua (FeS) màu xám.
Biết rằng, để cho phản ứng hoá hợp xảy ra hết người ta đã lấy dư lưu huỳnh. Tính khối lượng lưu huỳnh lấy dư.
15.5. Biết rằng canxi oxit (vôi sống) CaO hoá hợp với nước tạo ra canxi hiđroxit
(vôi tôi) Ca(OH)2, chất này tan được trong nước, cứ 56 g CaO hoá hợp vừa
đủ với 18 g O. Bỏ 2,8 g CaO vào trong một cốc lớn chứa 400 ml nước tạo
ra dung dịch Ca(OH)2, còn gọi là nước vôi trong.
a) Tính khối lượng của canxi hiđroxit.
b) Tính khối lượng của dung dịch Ca(OH)7, giả sử nước trong cốc là nước tinh khiết.
15.6. Đun nóng 15,8 g kali pemanganat (thuốc tím) KMnơ4 trong ống nghiệm để
điều chế khí oxi. Biết rằng, chất rắn còn lại trong ống nghiệm có khối lượng 12,6g ; khối lượng khí oxi thu được là 2,8g.
Tính hiệu suất của phản ứng phân huỷ.
( Hướng dẫn : Hiệu suất được tính như sau :
![]()
Trong bài tập này, lí thuyết là định luật bảo toàn khối lượng).
15.7. Còn có thể điều chế khí oxi bằng cách đun nóng kali clorat K (chất rắn màu trắng). Khi đun nóng 24,5 g KC
, chất rắn còn lại trong ống nghiệm có khối lượng là 13,45 g.
Tính khối lượng khí oxi thu được, biết hiệu suất của phản ứng phân huỷ là 80%.
(Xem hướng dẫn bài tập 15.6).
Xem thêm Phương trình hóa học tại đây

Trackbacks