B. Phần hướng dẫn giải – Đáp số – Chương 6 – Bài 43 : Pha chế dung dịch
43.1. Pha chế 100 ml dung dịch 0,4M :
– Phần tính toán :
+ Tìm số mol có trong dung dịch phải pha chế :
![]()
+ Tìm thể tích dung dịch 2M, trong đó có hoà tan 0,04 mol
:
![]()
– Phần pha chế:
+ Đong lấy 20 ml dung dịch 2M cho vào bình tam giác.
+ Thêm từ từ nước cất vào bình cho đủ 100 ml. Lắc đều, ta được 100 ml dung dịch 0,4M.
43.2.Pha chế 250 ml dung dịch NaCl 0,2M :
– Phần tính toán :
+ Tìm số mol NaCl có trong dung dịch cần pha chế :
![]()
+ Tìm thể tích dung dịch NaCl IM trong đó có hoà tan 0,05 mol NaCl:
![]()
– Phần pha chế:
+ Đong lấy 50 ml dung dịch NaCl 1M cho vào bình tam giác.
+ Thêm dần dần nước cất vào bình cho đủ 250 ml. Lắc đều, ta được 250 ml dung dịch NaCl 0,2M cần pha chế.
43.3. Tính toán và pha chế tương tự các bài tập 43.1, 43.2 ở trên
43.4. Pha chế 200 g dung dịch glucozơ 2% :
– Phần tính toán :
Tính khối lượng glucozơ cần dùng :
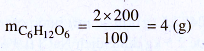
– Phần pha chế:
+ Cân lấy 4 g glucozơ cho vào bình tam giác.
+ Cân lấy 200 – 4 = 196 (g) nước cất, hoặc đong 196 ml nước cất, đổ vào bình tam giác. Lắc mạnh cho glucozơ tan hết, ta được 200 g dung dịch glucozơ 2%.
43.5.a) Cách tính toán và pha chế các dung dịch tương tự các bài tập 43.1,43.2 ở trên,
b) Cách tính toán và pha chế các dung dịch tương tự bài tập 43.4 ở trên.
43.6.a) Pha chế 500 ml dung dịch NaO 0,5M từ dung dịch NaCl 2M :
– Phần tính toán :
+ Tìm số mol NaCl có trong 500 ml dung dịch cần pha chế :
![]()
+ Tìm thể tích dung dịch NaCl 2M trong đó có hoà tan 0,25 mol NaCl;
![]()
– Phần pha chế:
+ Đong lấy 125 ml dung dịch NaCl 2M cho vào bình tam giác.
+ Thêm từ từ nước cất vào bình cho đủ 500 ml. Lắc đều, ta được 500 ml dung dịch NaCl 0,5M cần pha chế.
b) và c) : Cách pha chế 2 lít dung dịch 0,2M và 50 ml dung dịch
0,2M tương tự phần a) của bài tập này.
43.7. a) Pha chế 2,5 kg dung dịch NaCl 0,9% từ NaCl và nước cất:
– Phần tính toán :
Tìm khối lượng NaCl cần dùng để pha chế 2,5 kg dung dịch NaCl 0,9% :
![]()
– Phần pha chế:
+ Cân lấy 22,5 g Naơ tinh khiết cho vào chậu thuỷ tinh có dung tích vào khoảng 3 lít.
+ Đổ thêm 2500 – 22,5 = 2477,5 (g) (hoặc ml) nước cất vào chậu. Khuấy nhẹ cho muối tan hết, ta được 2,5 kg dung dịch NaCl 0,9%.
b) và c) : Cách tính toán và pha chế các dung dịch 4% và dung dịch
0,1% cũng tương tự phần a) của bài tập này.
43.8.Pha chế 50 ml dung dịch 1,5M :
– Phần tính toán :
+ Tìm số mol cẩn có để pha chế 50 ml dung dịch
1,5M :
![]()
+ Đặt X (ml) và y (ml) là thể tích của dung dịch 1M và
3M phải dùng. Số mol
cần phải lấy của mỗi dung dịch là 0,00lx và 0,003y. Ta có hệ phương trình đại số :
0,001x + 0,003y = 0,075
x + y = 50
Giải hệ phương trình, ta có : x = 37,5 và y = 12,5.
– Cách pha chế:
Đong lấy 37,5 ml dung dịch IM và 12,5 ml dung dịch H_{2}SO_{4} $ 3M cho vào bình tam giác, lắc đều, ta được 50 ml dung dịch
1,5M.
43.9. Pha chế 2 lít dung dịch NaOH 8%
– Phần tính toán :
+ Um khối lượng NaOH có trong 2 lít dung dịch NaOH 8% có khối lượng riêng là 1,1 g/ml:
![]()
+ Đặt x (ml) và y (ml) là thể tích dung dịch NaOH 3% và NaOH 10% cần phải lấy để pha chế. Khối lượng NaOH trong các dung dịch sẽ là :
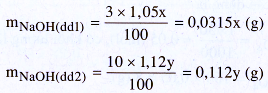
Ta có hệ phương trình đại số :
0,0315x + 0,112y = 176
x + y = 2000
Giải hệ phương trình, ta có : x = 569,3 và y = 1430,7.
– Phần pha chế: >
Đong lấy 569,3 ml dung dịch NaOH 3% và 1430,7 ml dung dịch NaOH 10% vào bình có dung tích 2,5 đến 3 lít. Trộn đều, ta được 2 lít dung dịch NaOH 8%, có khối lượng riêng là 1,10 g/ml.
Xem thêm B. Phần hướng dẫn giải – Đáp số – Chương 6 – Bài 44 : Luyện tập chương 6 Tại đây

Trackbacks