Đáp án Bài 6
6.1.
a) Số khối của photpho là 31 (đáp án B đúng).
b) Nguyên tử khối của photpho là 30,98 (đáp án A đúng).
c) Khối lượng mol nguyên tử của photpho là 30,98 g/mol (đáp án C đúng).
6.2. D
6.3. D
6.4.
a) Nguyên tử có 16 electron.
b)
c) Lớp electron ngoài cùng có 6 electron trong đó có 2 electron s và 4 electron p.
d) Đó là nguyên tử của một nguyên tố phi kim.
6.5.
Nguyên tố s là nguyên tố mà trong nguyên tử, electron cuối cùng được điền vào phân lớp s.
Nguyên tố p là nguyên tố mà trong nguyên tử, electron cuối cùng được điền vào phân lớp p.
Nguyên tố d là nguyên tố mà trong nguyên tử, electron cuối cùng được điền vào phân lớp d.
Nguyên tố f là nguyên tố mà trong nguyên tử, electron cuối cùng được điền vào phân lớp f.
6.6. Nguyên tử Y.
6.7.
a) Nguyên tử X.
b) Nguyên tử Z.
Ở đây mức năng lượng cao nhất là mức 3d. Vì vậy electron cuối cùng được điền vào phân lớp 3d (mức 4s thấp hơn mức 3d).
6.8.
a) Gọi X là số proton. Vì số proton bằng số electron nên X cũng là số electron. Theo đề bài, số nơtron bằng (x + 1). Từ đó ta có phương trình :
2x + x + 1 = 28
3x = 28 – 1 = 27
x = 9
Vậy số proton là 9, số nơtron là 10, số electron là 9.
b) Số khối A = 9 + 10 = 19.
c) Với 9 electron, cấu hình electron sẽ là .
d) Với Z = 9. Đó là nguyên tố flo (F).
6.9.
a) Cấu hình electron : → 1 electron ở lớp ngoài cùng.
b) Cấu hình electron : → 3 electron ở lớp ngoài cùng.
c) Cấu hình electron : → 4. electron ở lớp ngoài cùng.
d) Cấu hình electron : → 6 electron ở lớp ngoài cùng.
6.10.
Điện tích của electron :
=
C.
Proton mang điện tích dương :
=
C.
Hạt nhân cacbon có 6 proton, vậy điện tích của hạt nhân nguyên tử cacbon bằng :
q = .6 =
C.
6.11.

6.12.
a) 1 mol nhôm có nguyên tử nhôm.
10 mol nhôm có : .10 =
(nguyên tử nhôm),
b) Khối lượng mol nguyên tử nhôm :
![]()
6.13.

6.14.
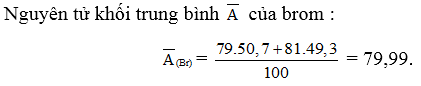
6.15.
Nguyên tố cần tìm thuộc nhóm VIIA → nguyên tử có 7e ở lớp ngoài cùng. Vì lớp thứ nhất chỉ chứa tối đa 2e nên nguyên tử của nguyên tố này phải có ít nhất 2 lớp electron (n ≥ 2).
+ Nếu n = 2, có 2 lớp e, số e ở các lớp là : 2,7 → nguyên tử gồm : 9p, 9e và 10n (tổng số hạt là 28, phù hợp đề bài).
+ Nếu n = 3, có 3 lớp e, số e ở các lớp là : 2, 8, 7 → vậy chỉ riêng số p + số e = 17 + 17 = 34 > 28 → trái với đề bài. Vậy nguyên tố cần tìm có Z = 9 với cấu hình electron : .
6.16.
Trong những nguyên tố có số hiệu nguyên tử từ Z = 1 đến Z = 36, chỉ có nguyên tố neon là có cấu hình electron thoả mãn 2 điều kiện của đề bài.
Ne :
Các nguyên tố khác :
He : bên ngoài chỉ có 2e.
Ar : 2/8/8 lớp ngoài cùng có 8e, nhưng lớp thứ 3 chưa đủ số e tối đa.
Kr : 2/8/18/8 lớp ngoài cùng có 8e, nhưng lớp thứ 4 chưa đủ số e tối đa.



Trackbacks