Bài 19 Luyện tập
19.1. Loại phản ứng hoá học nào sau đây luôn luôn là phản ứng oxi hoá – khử ?
A. phản ứng hoá hợp.
B. phản ứng phân huỷ.
C. phản ứng thế.
D. phản ứng trao đổi.
19.2. Loại phản ứng hoá học nào sau đây luôn luôn không phải là phản ứng oxi hoá – khử ?
A. phản ứng hoá hợp.
B. phản ứng phân huỷ.
C. phản ứng thế.
D. phản ứng trung hoà.
19.3. Cho các phản ứng sau :
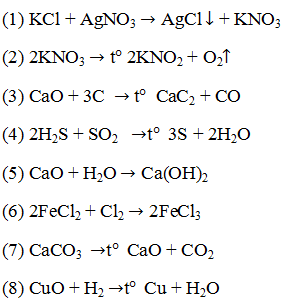
Dãy nào sau đây chỉ gồm các phản ứng oxi hoá – khử ?
A. (1), (2), (3), (4), (5).
B. (2), (3), (4), (5), (6).
C. (2), (3), (4), (6), (8).
D. (4), (5), (6), (7), (8).
19.4. Phản ứng trong đó có sự thay đổi số oxi hoá của các nguyên tử trong cùng một phân tử gọi là phản ứng oxi hoá – khử nội phân tử.
Phản ứng nào sau đây thuộc loại trên ?
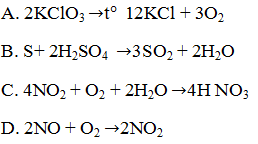
19.5. Phản ứng nào cho dưới đây chỉ xảy ra sự thay đổi số oxi hoá của một nguyên tố ?
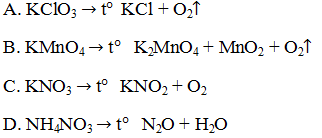
19.6. Cho sơ đồ phản ứng :
—>
Cân bằng PTHH của phản ứng trên. Các hệ số tương ứng với phân tử các chất là dãy số nào sau đây ?
A. 3, 14, 9, 1, 7.
B. 3, 28, 9, 1, 14.
C. 3, 26, 9, 2, 13.
D. 2, 28, 6, 1, 14.
19.7. Trong phản ứng :
+ HCl → t°
Số phân tử HCl đóng vai trò chất khử bằng k lần tổng số phân tử HCl tham gia phản ứng. Giá trị của k là
A. 3/14
B. 4/7
C. 1/7
D. 3/7
19.8. Cho phản ứng :
—>
+ NO↑ +
Hệ số tối giản của và
trong phản ứng trên lần lượt là
A. 12 ; 4.
B. 16; 4.
C. 10 ; 6.
D. 8 ; 2.
19.9.
Trong phản ứng đốt cháy tạo ra sản phẩm CuO,
và
thì một phân tử
sẽ
A. nhận 13e.
B. nhận 12e.
C. nhường 13e.
D. nhường 12e.
19.10.
Cho 2,24 g sắt tác dụng với dung dịch HCl dư. Khí sinh ra cho đi qua ống đựng 4,2 g CuO được đốt nóng. Xác định khối lượng của chất rắn ở trong ống sau khi phản ứng xảy ra hoàn toàn.
19.11. Nguyên tố nitơ trong các hợp chất có số oxi hoá thấp nhất là -3 và cao nhất là +5. Xác định số oxi hoá của nitơ trong các hợp chất sau và xét xem trong hợp chất nào nitơ chỉ có tính oxi hoá, trong hợp chất nào nitơ chỉ có tính khử ?
a) .
b) .
19.12. Nhúng thanh kẽm vào 100 ml dung dịch 0,1M. Tính khối lượng bạc kim loại được giải phóng và khối lượng kẽm đã chuyển vào dung dịch.
19.13. Cho 2,6 g bột kẽm vào 100 ml dung dịch 0,75M. Lắc kĩ cho đến khi phản ứng kết thúc. Xác định số mol của các chất trong dung dịch thu được.
19.14. Hỗn hợp khí A gồm clo và oxi. A phản ứng vừa hết với hỗn hợp gồm 4,8 g magie và 8,1 g nhôm tạo ra 37,05 g hỗn hợp các muối clorua và oxit của 2 kim loại. Tính số mol clo và oxi trong A.
19.15. Một dung dịch X có chứa 46,5 g hỗn hợp phản ứng vừa đủ với dung dịch
, thu được 114,8 g kết tủa và dung dịch Y. Tính khối lượng muối trong dung dịch Y.




Comments mới nhất