I.KIẾN THỨC CẦN NHỚ
1.Tính chất vật lí
-Rượu etylic là chất lỏng, không màu, sôi ở 78,3°c, nhẹ hơn nước, tan vô hạn trong nước, hoà tan được nhiều chất: iot, benzen,…
-Số ml rượu etylic có trong 100 ml hỗn hợp (rượu + nước) gọi là độ rượu.
2.Tính chất hóa học
a.Phản ứng cháy
Rượu etylic tác dụng mạnh với oxi, tạo khí cacbonic và hơi nước.
![]()
b.Rượu etylic phản ứng với natri
Rượu etylic tác dụng được với natri giải phóng khí, đó là khí hiđro.
2CH3 – CH2 – OH + 2Na → 2CH3 – CH2 – ONa + H2
c.Phản ứng với axit axetic (Xem bài 45)
3.Ứng dụng
-Cao su tổng hợp.
-Rượu bia.
-Dược phẩm.
-Pha nước hoa.
4.Điều chế
Rượu etylic thường được điều chế theo hai cách:
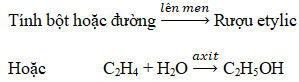
II.GIẢI BÀI TẬP
Bài 1. Trang 139 sách giáo khoa hóa học 9
Chọn phương án D: Rượu etylic phản ứng được với natri vì trong phân tử có nhóm -OH.
Bài 2. Trang 139 sách giáo khoa hóa học 9
Chất tác dụng được với Na là: CH3 – CH2 – OH
Phương trình hóa học:
2CH3 – CH2 – OH + 2Na → 2CH3 – CH2 – ONa + H2↑
Bài 3. Trang 139 sách giáo khoa hóa học 9 hóa học 9
-Ống 1 đựng rượu etylic.
Ông 1 có phản ứng của rượu với Na:
Phương trình phản ứng:
2CH3 – CH2 – OH + 2Na → 2CH3 – CH2 – ONa + H2 ↑
-Ống 2 đựng rượu 96°.
Ống 2 có phản ứng của rượu và nước với Na.
2CH3 – CH2 – OH + 2Na → 2CH3 – CH2 – ONa + H2 ↑
2Na + 2H2O → 2NaOH + H2 ↑
-Ống 3 đựng nước.
Ống 3 có phản ứng của nước với Na.
2Na + 2H2O2 → 2NaOH + H2 t
Bài 4. Trang 139 sách giáo khoa hóa học 9
a.Giải thích ý nghĩa của các số trên.
Rượu 45° có nghĩa là trong 100 ml hỗn hợp rượu nước có 45mil rượu nguyên chất. Tương tự như vậy đối với rượu 18° và 12°.
b.Tính số ml rượu etylic có trong 500ml rượu 45°.
![]()
c.Có thể pha được bao nhiêu lít rượu 25° từ 500ml rượu 45°.
Áp dụng phương pháp đường chéo ta có:
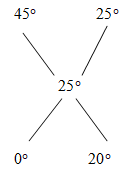
Gọi V là thể tích nước có độ rượu là 0°, ta có tỷ lệ:
500/ V = 25/20 => V = 400 (ml)
Thể tích rượu bỏ qua hiệu ứng thể tích là 900ml = 0,9 (l)
Bài 5. Trang 139 sách giáo khoa hóa học 9
Số mol rượu = 9,2 / 46 = 0,2 (mol)
a.Tính thể tích khí CO2 tạo ra ở điều kiện tiêu chuẩn.
C2H5OH + 3O2 → 2CO2↑ + 3H2O
0,2mol 0,6mol 0,4mol
VCO2 = 0,4 x 22,4 = 8,96 (l)
b.Tính thể tích không khí (ở điều kiện tiêu chuẩn).
VO2= 0,6 x 22,4 = 13,44 (l) => Vkk = 13,44 x 5 = 67,2 (l)

Comments mới nhất