I.KIẾN THỨC CẦN NHỚ
1.Tính chất vật lí
-Chất khí không màu, không mùi, không vị, ít tan trong nước.
-Nhẹ hơn không khí (d = 26/29)
2.Công thức cấu tạo
So sánh cấu tạo giữa etilen và axetilen:
-Giống: đều là hiđrocacbon, đều có liên kết kém bền trong phân tử.
-Khác: etilen có 1 liên kết kém bền, axetilen có 2 liên kết kém bền trong phân tử.
3.Tính chất hóa học
a.Phản ứng cháy
![]()
b.Phản ứng làm mất màu dung dịch brom (phản ứng cộng)
CH ≡ CH + Br – Br → Br – CH = CH – Br
Br – CH = CH – Br + Br – Br → Br2CH – CHBr2
4.Ứng dụng
-Nhiên liệu trong đèn xì oxi-axetilen để hàn cắt kim loại.
-Trong công nghiệp, axetilen là nguyên liệu để sản xuất poli, cao su, axit axetic và nhiều hóa chất khác.
5.Điều chế
-Từ canxicacbua (CaC2)
(Trong phòng thí nghiệm và công nghiệp).
CaC2 + 2H2O → C2H2 + Ca(OH)2
-Phương pháp hiện đại điều chế C2H2 là nhiệt phân metan ở nhiệt độ cao.
II.GIẢI BÀI TẬP
Bài 1. Trang 122 sách giáo khoa hóa học 9
a.CH ≡ CH và CH ≡ C – CH3 có liên kết 3.
b.Chất làm mất màu dung dịch brom.
CH ≡ CH;
CH2 = CH2;
CH = C – CH3.
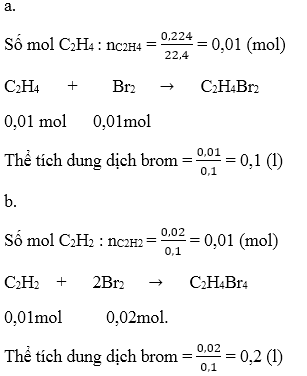
Bài 2. Trang 122 sách giáo khoa hóa học 9
Bài 3. Trang 122 sách giáo khoa hóa học 9
Suy luận tương tự bài 2 ở trên.
0,1 lít khí C2H2 có thể làm mất màu 50 x 2 = 100 (ml) dung dịch brom.
Bài 4. Trang 122 sách giáo khoa hóa học 9
a.Tính phần trăm thể tích của mỗi khí trong hỗn hợp.
CH4 + 2O2 → CO2 ↑ + 2H2O (1)
xml 2xml xml
C2H2 + 5/2 O2 → 2CO2 + H2O (2)
yml 2,5yml 2yml
Thể tích hai khí là: x + y = 28 (I)
Thể tích khí oxi: 2x + 2,5y = 67,2 (II)
Suy ra y = 22,4 (ml) và X = 28 – 22,4 = 5,6 (ml)
b.Tính thể tích khí CO2 sinh ra.
V= x+ 2y = 5,6 + (2 x 22,4) = 50,4 (l)
Bài 5. Trang 122 sách giáo khoa hóa học 9
a.Phương trình hóa học.
C2H4 + Br2 → C2H4Br2
xmol xmol
C2H2 + 2Br2 → C2H2Br4
ymol 2ymol
b.Tính % thể tích của mỗi khí trong hỗn hợp.
x + y = 0,56 / 22,4 = 0,025 (mol) (1)
Số mol Br2 = x + 2y = 5,6 / 160 = 0,035 (mol) (2)
y = 0,01 (mol) và x = 0,015 (mol)
Thể tích C2H4= 0,015 x 22,4 = 0,336 (l)
Thể tích của C2H2 = 0,01 x 22,4 = 0,224 (l)

Comments mới nhất