Bài 3 Luyện tập
3.1. Liti trong tự nhiên có hai đồng vị:

Nguyên tử khối trung bình của liti là
A. 7.
B. 6,93.
C. 6,07.
D. 6.
3.2. Phát biểu nào sau đây đúng?
A. Chỉ có hạt nhân nguyên tử oxi mới có 8 nơtron.
B. Chỉ có hạt nhân nguyên tử oxi mới có 8 electron.
C. Chỉ có hạt nhân nguyên tử oxi mới có 8 proton.
D. Chỉ có ion mới có 10 electron.
3.3. Kim loại M có số khối bằng 55. Tổng số các hạt cơ bản trong ion bằng 79. Kí hiệu nguyên tử của kim loại M là
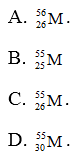
3.4. Dưới đây là thành phần phần trăm của các đồng vị thuộc hai nguyên tố Ar và
K.

a) Hãy tính nguyên tử khối trung bình của Ar và K (một cách gần đúng coi nguyên tử khối của các đồng vị trùng với số khối của chúng).
b) Trong trường hợp này hãy giải thích tại sao Ar có số đơn vị điện tích hạt nhân (số thứ tự) nhỏ hơn K mà lại có nguyên tử khối lớn hơn ?
3.5.
a) Khối lượng mol nguyên tử là gì ?
b) Hãy cho biết mối quan hệ giữa nguyên tử khối và khối lượng mol nguyên tử.
Cho thí dụ cụ thể.
3.6. Khi điện phân 75,97 g NaCl (muối ăn tinh khiết) nóng chảy người ta thu được 29,89 g Na. Hãy xác định nguyên tử khối của clo (cho biết nguyên tử khối của natri bằng 22,99).
3.7.

Hãy viết công thức của các loại phân tử liti clorua khác nhau.
3.8. Tổng số hạt proton, nơtron, electron trong 2 nguyên tử kim loại X và Y là 142, trong đó tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 42. Số hạt mang điện của nguyên tử Y nhiều hơn của X là 12. Xác định hai kim loại X và Y.
3.9. Tổng số hạt proton, nơtron, electron trong nguyên tử của một nguyên tố là 34. Biết rằng tỉ số N/Z (N là tổng số hat nơtron, Z là tổng số hat proton) của các nguyên tố có Z = 1 đến Z = 20 có giá trị lớn nhất là 1,2. Xác định nguyên tử khối của nguyên tố đó.



Comments mới nhất